IVD ürünleri, sağlık durumlarını teşhis etmek, tedavi etmek veya önlemek için kullanılan cihazlar ve sistemlerdir. Kan, tükürük veya doku gibi biyolojik örneklerin toplanması ve incelenmesinde kullanılmak içindir. Numuneler burnun içinden veya boğazın arkasından veya damardan veya parmak ucundan alınabilir.
IVD ürünlerinin noninvaziv olduğuna dikkat etmek önemlidir. Örneğin,
Poclight HSCL-5000 Mikro homojen kemilüminesans immunoassay analizörü
.
Ancak yine de tıbbi cihaz olarak kabul edilirler ve bu nedenle aynı kontrollere tabidirler. Tıbbi cihazlar, aşağıdaki amaçlarla insanlar için kullanılması amaçlanan herhangi bir alet, cihaz, yazılım veya ilgili cihazdan oluşur:
·
Hastalık veya yaralanmayı teşhis etmek, önlemek, izlemek veya tedavi etmek.
·
Yaşamı desteklemek veya sürdürmek.
·
Konsepsiyonun düzenlenmesi.
·
Tıbbi cihazların dezenfekte edilmesi.
·
İnsanlardan biyolojik numuneler toplayarak tıbbi amaçlı bilgi sağlamak.
In Vitro Diagnostics üreticileri, girmek istedikleri pazar(lar)a bağlı olarak Avrupa Birliği, Birleşik Krallık ve ABD'nin düzenleyici gereksinimlerini karşılamalıdır.
Bu gereksinimler, AB'de İn Vitro Tanı Yönetmeliği (IVDR) (EU) 2017/746 ve Birleşik Krallık'ta Birleşik Krallık Tıbbi Cihazlar Yönetmeliği (UK MDR) 2002'yi içerir. Amerika Birleşik Devletleri'nde, IVD ürünleri Federal Gıda, İlaç ve Kozmetik Yasası'nın (FD&C Yasası) 201(h) bölümünde tanımlanmıştır; bu cihazlar ayrıca Halk Sağlığı Hizmeti Yasası'nın 351. bölümüne ve 1988 tarihli Klinik Laboratuvar İyileştirme Değişiklikleri (CLIA) kapsamındaki sınıflandırmaya tabi olabilir.
IVDR'ye göre, bir IVD ürünü, "ister tek başına ister kombinasyon halinde kullanılsın, amaçlanan bir reaktif, reaktif ürün, kalibratör, kontrol malzemesi, kit, alet, aparat, ekipman parçası, yazılım veya sistem olan herhangi bir tıbbi cihaz" olarak tanımlanır. üretici tarafından insan vücudundan elde edilen kan ve doku bağışları da dahil olmak üzere örneklerin in vitro incelenmesi için kullanılmak üzere…”
Uzmanlar, tüm klinik kararların yaklaşık %70'inin IVD ürünleri kullanılarak verildiğini tahmin ediyor.
IVD Ürünlerine Örnekler
Hamilelik testleri, COVID-19 testleri ve HIV testleri IVD ürünlerine örnektir. Poclight HSCL-5000 Micro CLIA Analyzer IVD cihazlarının diğer örnekleri şunları içerir:
·
Kanser teşhisi
· Tiroid teşhisi
· Enflamasyon teşhisi
·
İmmünolojik testler
· ...
Tıbbi numuneler için üretilen kaplar da IVD ürünleridir. Dünya Sağlık Örgütü'ne göre, bugün IVD testi için 40.000'den fazla ürün mevcuttur. Bunlar, geleneksel laboratuvar testlerinden bakım noktası testlerine kadar değişebilir.
IVD Sınıflandırması
Amerika Birleşik Devletleri'nde FDA, IVD ürünleri de dahil olmak üzere tüm tıbbi cihazları Sınıf I, Sınıf II veya Sınıf III olarak sınıflandırır. Cihazın sınıflandırması, içerdiği riske ve ürünün güvenliğini garanti altına almak için gereken düzenleyici kontrol düzeyine göre değişiklik gösterecektir. Buna göre, IVD sınıflandırması, üreticinin ürünlerini piyasaya sürmek için izlemesi gereken pazarlama öncesi süreci belirleyecektir.
·
Sınıf I ürünler, düşük ila orta risk olarak kabul edilir ve genel kontroller gerektirir.
·
Sınıf II ürünler orta ila yüksek risk olarak kabul edilir ve genel kontroller ve Özel Kontroller gerektirir.
·
Sınıf III ürünler yüksek riskli olarak kabul edilir ve genel kontroller ve Pazar Öncesi Onay (PMA) gerektirir.
Cihaz sınıfı arttıkça düzenleyici kontrollerin de arttığına dikkat etmek önemlidir. Sınıf I IVR cihazları en az düzenleyici kontrole tabiyken, Sınıf III IVR cihazları en katı gereksinimlere sahiptir. Amerika Birleşik Devletleri'nde In Vitro Diagnostic ürünlerini piyasaya sürmek isteyen Yaşam Bilimleri şirketleri, FDA'nın “Tıbbi Cihazınızı Sınıflandırın” kaynağına başvurabilirler.
Avrupa Birliği'nde mevzuata uygunluğu sağlamak mı istiyorsunuz? IVDR, 2021'de aşağıdaki gibi iyileştirmeleri içerecek şekilde yükseltildi:
·
Cihaz izlenebilirliği, kaydı ve uygun etiketlemenin doğrulanmasıyla ilgili üreticiler, ithalatçılar ve distribütörler için net yükümlülükler. Bu, benzersiz bir cihaz tanımlayıcısı (UDI) üzerine kurulmuş bir izlenebilirlik sistemini içerir.
·
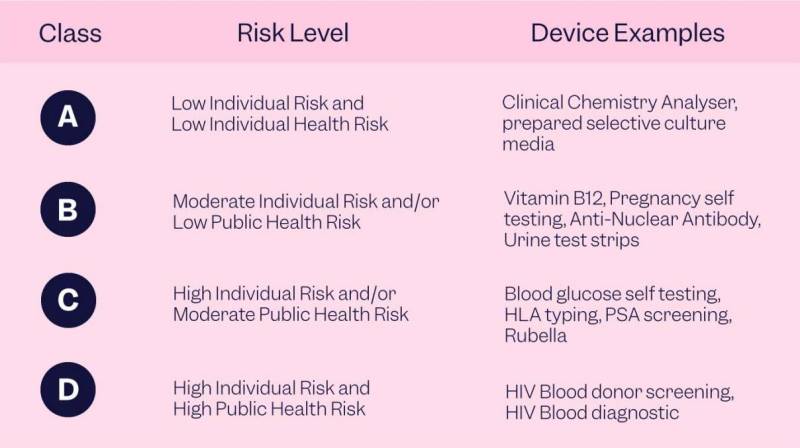
Dört risk sınıfından oluşan bir sınıflandırmanın tanıtılması. A Sınıfı cihazlar düşük bireysel ve halk sağlığı riski, B Sınıfı cihazlar orta düzeyde bireysel ve/veya düşük halk sağlığı riski, C Sınıfı cihazlar yüksek bireysel risk ve/veya orta düzeyde halk sağlığı riski ve D Sınıfı cihazlar yüksek bireysel risk ve yüksek halk sağlığı riski.
·
Yüksek riskli IVD cihazları için daha sıkı kontroller.
·
Belirli bir dizi kriteri güçlendirerek onaylanmış kuruluşların (veya bağımsız üçüncü taraf uygunluk değerlendirme kuruluşlarının) garantili gözetimi.
·
AB'deki (EUDAMED olarak adlandırılan) tıbbi cihazlarla ilgili kapsamlı bir veri tabanı ile daha fazla şeffaflık.
·
Özellikle piyasa gözetimi söz konusu olduğunda AB ülkeleri arasında daha fazla koordinasyon ile güçlendirilmiş klinik kanıt ve performans değerlendirme düzenlemeleri.
·
Daha güçlü üretici pazar sonrası gözetim gereksinimleri.
·
Aynı kurum içinde üretilen ve kullanılan “kurum içi cihazlar” veya IVD ürünleri için özel gereksinimler.
Bir IVD ürününün güvenli ve etkili bir şekilde pazarlanması çok önemlidir ve yürürlükteki düzenlemeleri anlamak ideal bir ilk adımdır.
Çözüm
IVD ürünleri, çeşitli sağlık koşullarına karşı kritik bir savunma hattıdır. In Vitro Diagnostics'in güvenliği ve kalitesi esastır, bu nedenle üreticinin mevzuata uygunluğu bu kadar önemlidir. Poclight, CE ve ISO sertifikalıdır ve testi sorunsuz hale getirmek için eksiksiz bir reaktif ürün yelpazesine sahiptir.

 English
English français
français русский
русский español
español português
português العربية
العربية 日本語
日本語 Türkçe
Türkçe हिंदी
हिंदी Indonesia
Indonesia 







 IPv6 Ağ Desteklendi |
IPv6 Ağ Desteklendi | 